Exercice pro Fiche véto
La nouvelle cascade dite du « hors AMM »
La nouvelle cascade dite du « hors AMM », fixée par le nouveau règlement européen 2019/6 « médicament vétérinaire », est plus simple dans l’ordre des recours possibles « hors AMM ». Dès le premier niveau, le vétérinaire peut recourir à tous les médicaments vétérinaires autorisés (avec AMM) dans l’UE pour un usage « dans l’AMM » ou « hors AMM ».
La cascade est-elle devenue un grand lac avec en aval quelques petites retenues ? L’image n’est pas fausse. Car la nouvelle cascade dite du « hors AMM » qui découle de l’application des articles 112 à 115 du règlement 2019/6 « médicament vétérinaire » [1] applicable depuis le 28 janvier 2022 a été, à la demande des vétérinaires, très simplifiée en regroupant trois niveaux de l’ancienne cascade en un seul.
Dès le premier niveau de la cascade, quand le vétérinaire n’a pas de médicament autorisé et approprié pour l’espèce ou l’indication visées, il peut d’emblée recourir à tous les médicaments avec une AMM vétérinaire valable en France ou, hors de France, dans l’Union européenne (UE), en vue d’un usage conforme à leur AMM ou « hors AMM », dans une autre espèce ou une autre indication que celles mentionnées dans leurs résumés des caractéristiques du produit (RCP).
Les importations
Les importations sont possibles depuis d’UE dès le premier niveau. Toutefois, l’importation en France depuis un autre État membre nécessite toujours une autorisation d’importation de l’Agence nationale du médicament vétérinaire (ANMV). Le formulaire de demande d’importation, dans lequel le vétérinaire justifie le recours, est téléchargeable sur le site internet de l’ANMV. L’Agence répond en 20 jours maximum aux demandes d’importation qui peuvent lui être transmises par courriel (+ 15 jours si des informations complémentaires sont requises).
Dans les productions animales, le vétérinaire recourt d’abord à un médicament déjà autorisé dans au moins une espèce productrice de denrées alimentaires ou contenant des substances autorisées (tableau 1 au règlement LMR). Cela garantit la fixation d’une limite maximale de résidus (LMR) dans au moins une denrée d’une espèce animale car cela reste un prérequis obligatoire dans les productions animales.
Les deux autres niveaux de la cascade sont peu modifiés avec un recours possible ensuite à un médicament humain (AMM valable en France), puis à une préparation magistrale (sans AMM).
Enfin, nouveauté au dernier niveau de la cascade, le vétérinaire peut recourir à l’importation d’un médicament vétérinaire autorisé dans un pays tiers dans l’espèce et l’indication visées, à l’exception des vaccins et des autres médicaments immunologiques. Comme précédemment, il convient alors de solliciter une autorisation d’importation de l’ANMV.
Le nouvel ordre de la cascade
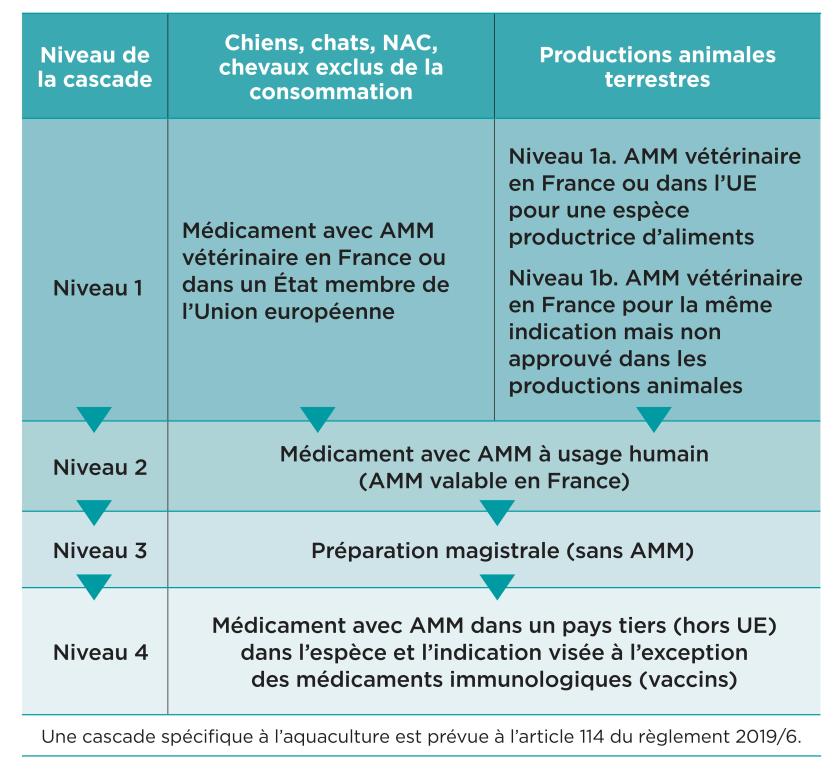

Les clarifications du ministère de l’Agriculture
Dans une instruction technique du 19 juin 2023, le ministère de l’Agriculture a beaucoup clarifié les notions de médicament autorisé, (in)approprié ou (in)disponible qui ouvrent ou pas à l’accès à la cascade. Le recours à la cascade n’est en effet possible qu’en l’absence de médicament disponible, autorisé en France et approprié :
-
un médicament est non disponible en cas de rupture déclarée par le titulaire d’AMM, et non lors d’une rupture dans le stock du vétérinaire ou en centrale. Toutefois, en cas d’urgence, le vétérinaire peut engager la cascade sans attendre une livraison ;
-
la notion de médicament approprié ou non est établie par le prescripteur sur des critères scientifiques ou sanitaires, mais en aucun cas économiques ;
-
si le vétérinaire juge qu’un médicament autorisé dans l’espèce et l’indication n’est pas approprié, il devrait pouvoir le justifier sur la base d’avis scientifiques (notamment de l’ANMV), de la bibliographie ou, à défaut, des déclarations de pharmacovigilance pour « manque d’efficacité » ;
-
le recours « hors AMM » à la phytothérapie ou à l’homéopathie — important pour l’agriculture biologique — est considéré d’emblée comme approprié même si des médicaments chimiques ou allopathiques avec AMM sont disponibles.
LMR
Autre nouveauté importante pour les productions animales, l’instruction n’exige plus que la LMR de la substance active soit fixée dans la denrée concernée par l’usage « hors AMM ». La France s’aligne ainsi sur la position européenne. Une substance active sans aucune LMR lait peut donc être utilisée chez les femelles laitières, mais seulement si l’inscription des LMR de la substance active dans le règlement LMR 37/2010 n’est pas associée à une contre-indication d’emploi chez les laitières. Si le médicament ne mentionne pas une utilisation chez une femelle laitière, il convient donc de vérifier cette interdiction éventuelle qui figure alors dans le tableau 1 des substances autorisées listées au règlement LMR 37/2010. Dans le cadre du contrôle des résidus, le règlement européen 2018/470 précise d’ailleurs quelle est la LMR à appliquer dans le cadre de la cascade en s’appuyant sur les LMR des denrées et des espèces animales les plus proches.
Temps d’attente en cascade
Les temps d’attente en cascade sont fixés par le vétérinaire (sous sa responsabilité). Ils ne sont pas modifiés en cas de changement d’indication sans changement d’espèce. En cas de changement d’espèce (ou implicitement en cas d’augmentation des doses ou de la durée du traitement), ils sont a minima multipliés par 1,5 fois le temps d’attente le plus long dans la denrée concernée (viande, lait ou oeufs) pour une autre espèce, avec un arrondi au nombre de jours entiers le plus proche.
Le temps d’attente viandes ou lait est de 1 jour s’il est nul pour les autres espèces. Un maintien est possible à zéro jour seulement dans la viande pour des espèces appartenant à la même famille taxonomique : les bovidés (bovins, ovins, caprins), les suidés (porcs, sangliers), les phasianidés (Gallus gallus, dindes, cailles, faisans, perdrix), les équidés (chevaux, ânes), …
Dans les autres cas, les temps d’attente sont a minima de 28 jours dans la viande, 7 jours dans le lait et 10 jours dans les oeufs.
L’application de ces temps d’attente minimaux ne dégage pas la responsabilité du vétérinaire. Ces temps d’attentes s’appliquent aussi aux vaccins et aux médicaments homéopathiques avec AMM.
Et les équidés ?
Les équidés exclus de la consommation humaine sont considérés comme des animaux de compagnie, sans restriction particulière. Le vétérinaire peut donc exclure définitivement l’équidé de la consommation humaine si cela lui apparaît nécessaire pour le soigner en mentionnant cette exclusion dans le livret d’identification et sur la base Sire.
Pour les équidés non exclus de la consommation humaine, la réglementation permet au vétérinaire de recourir à une liste de 88 substances sans aucune LMR, interdites dans les productions animales, mais « essentielles aux équidés ». Dans ce cas, le vétérinaire réalise toujours lui-même la première administration et mentionne l’exclusion temporaire de six mois de la consommation humaine dans le livret ainsi que dans base Sire.
Les sanctions possibles
Les poursuites contre les infractions à la cascade sont possibles sous trois angles : administratif, pénal et disciplinaire.
Les poursuites administratives peuvent aller dans les productions animales jusqu’à la séquestration et la destruction des animaux ou de leurs produits (article L. 234-3 du Code rural et de la pêche maritime), ou jusqu’à l’exclusion d’un équidé de la consommation humaine s’il ne l’était pas déjà.
Les poursuites pénales sont envisageables en cas d’infraction aux dispositions sur les LMR, les temps d’attente minimaux, les substances essentielles aux équidés, jusqu’à 150 000 € d’amende et 2 ans de prison (article L. 5442-10 du Code de la santé publique).
Enfin, des poursuites disciplinaires peuvent aussi être engagées auprès des Conseils régionaux de l’Ordre des vétérinaires.
